Алгоритм составления уравнений химических реакций
Для начала составим схему химической реакции. Например, образование оксида магния (MgO) в процессе горения магния (Mg) в кислороде (O₂). Обозначим реагенты и продукт реакции:
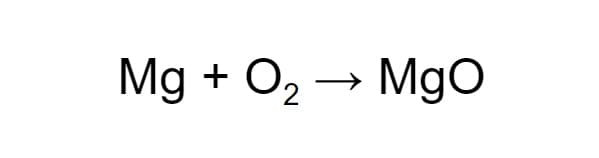
Чтобы схема стала уравнением, нужно расставить коэффициенты. В левой части схемы два атома кислорода, а в правой — один. Уравняем их, увеличив число молекул продукта:
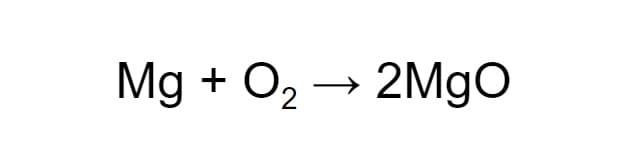
Теперь число атомов кислорода до и после реакции одинаковое, а число атомов магния — нет. Чтобы уравнять их, добавим ещё одну молекулу магния. Когда количество атомов каждого из химических элементов в составе веществ уравнено, вместо стрелки можно ставить равно:
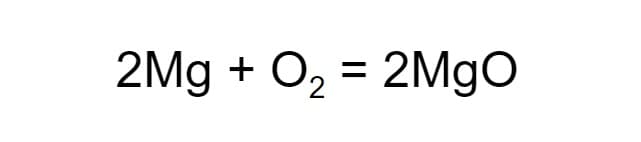
Уравнение химической реакции составлено.
Рассмотрим реакцию разложения. Нитрат калия (KNO₃) разлагается на нитрит калия (KNO₂) и кислород (О₂):
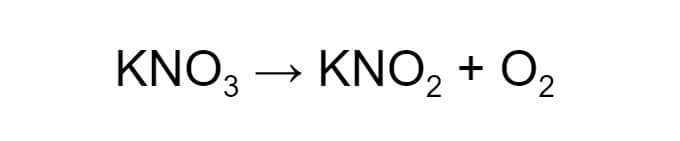
В обеих частях схемы по одному атому калия и азота, а атомов кислорода до реакции 3, а после — 4. Необходимо их уравнять.
Для начала удвоим коэффициент перед реагентом:
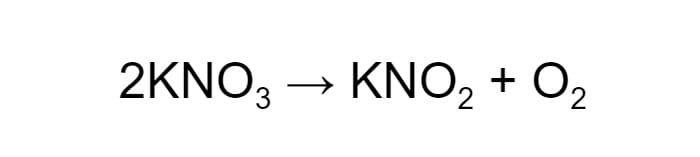
Теперь в левой части схемы шесть атомов кислорода, два атома калия и два атома азота. В левой по-прежнему по одному атому калия и азота и четыре атома кислорода. Чтобы уравнять их, в правой части схемы нужно удвоить коэффициент перед нитритом калия.
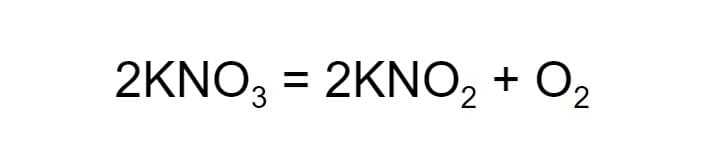
Снова посчитаем число атомов каждого химического элемента в составе веществ до и после реакции: два атома калия, два атома азота и шесть атомов кислорода. Равенство достигнуто.
Коэффициенты в уравнениях химических реакций
Чтобы составить уравнение химической реакции, важно правильно подобрать коэффициенты перед формулами веществ. Коэффициент в химических уравнениях означает число молекул (формульных единиц) вещества, необходимое для реакции
Он обозначается числом перед формулой (например, 2NaCl в последнем примере)
Коэффициент в химических уравнениях означает число молекул (формульных единиц) вещества, необходимое для реакции. Он обозначается числом перед формулой (например, 2NaCl в последнем примере).
Коэффициент не следует путать с индексом (числом под символом химического элемента, например, О₂). Индекс обозначает количество атомов этого элемента в молекуле (формульной единице).
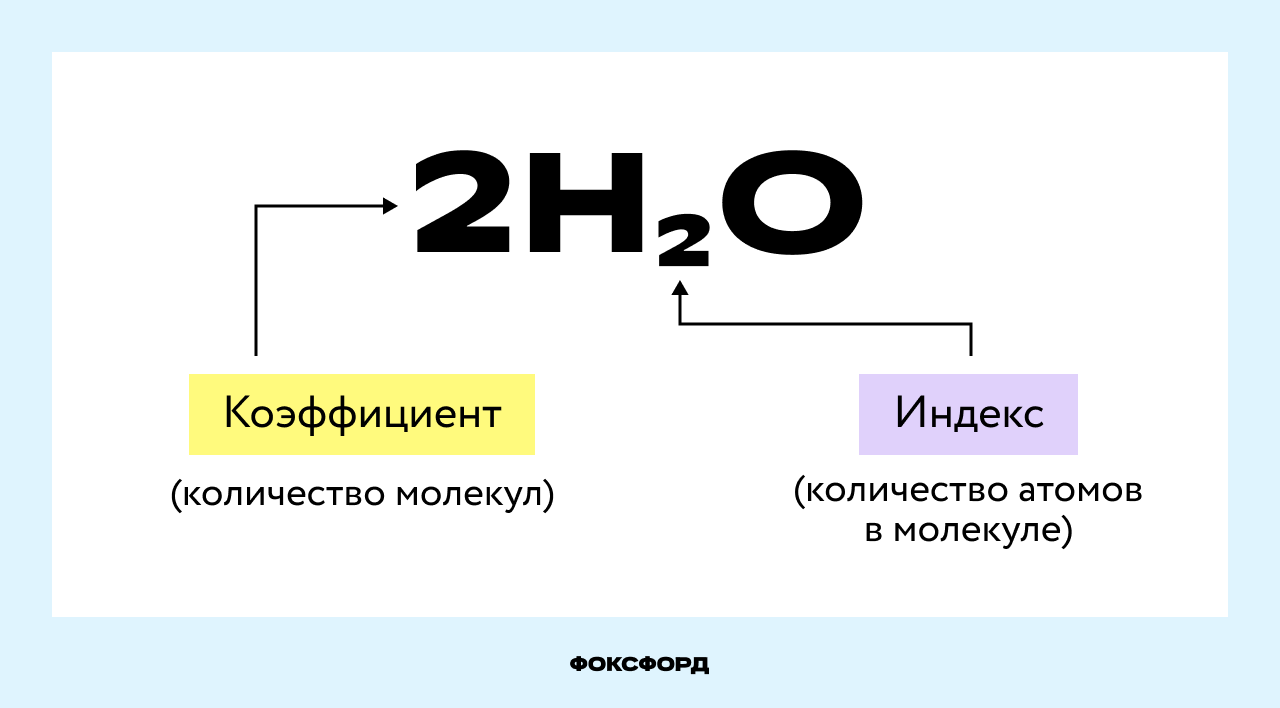
Чтобы узнать общее число атомов элемента в формуле, нужно умножить его индекс на коэффициент вещества. В примере на картинке (2H₂O) — четыре атома водорода и два кислорода.
Подобрать коэффициент — значит определить, сколько молекул данного вещества должно участвовать в реакции, чтобы она произошла. Далее мы расскажем, как это сделать.
Что такое химические уравнения
Когда химические вещества вступают во взаимодействие, химические связи между их атомами разрушаются и образуются новые, уже в других сочетаниях. В результате одни вещества превращаются в другие.
Рассмотрим реакцию горения метана, происходящую в конфорке газовой плиты:
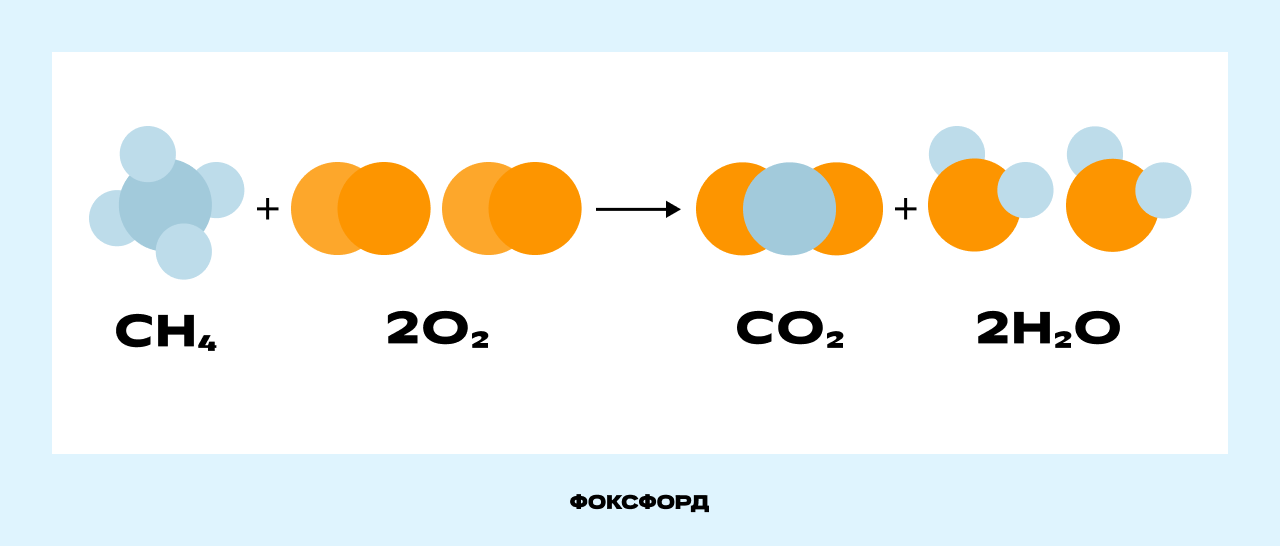
Молекула метана (CH₄) и две молекулы кислорода (2O₂) вступают в реакцию, образуя молекулу углекислого газа (CO₂) и две молекулы воды (2H₂O). Связи между атомами углерода (С) и водорода (H) в метане, а также между атомами кислорода (O) разрываются, и образуются новые связи между атомами углерода и кислорода в молекуле углекислого газа (CO₂) и между атомами водорода и кислорода в молекуле воды (H₂O).
Картинка даёт наглядное представление о том, что произошло в ходе реакции. Но зарисовывать сложные химические процессы такими схемами неудобно. Вместо этого учёные используют уравнения химических реакций.
Химическое уравнение — это условная запись химической реакции с помощью формул и символов.
Их записывают в виде схемы, в которой отражён процесс превращения. В левой части располагаются формулы реагентов — веществ, вступающих в реакцию. Завершается уравнение продуктами реакции — веществом или веществами, которые получились в результате.
Новые вещества образуются потому, что изменяются связи между атомами, но сами атомы не возникают из ниоткуда и не исчезают в никуда. На рисунке видно, что атом углерода из состава метана перешёл в состав углекислого газа, атом водорода — в состав воды, а атомы кислорода распределились между молекулами углекислого газа и воды. Число атомов не изменилось.
Согласно закону сохранения массы, общая масса реагентов всегда равна общей массе продуктов реакции. Именно поэтому запись химической реакции называют уравнением.
<<Форма демодоступа>>
Похожие ГДЗ Химия 8 класс
Решебник №2
Предыдущее
Следующее
Органические и неорганические соединения окружают человека постоянно, с самого рождения. Чтобы изучить большую их часть, требуется потратить годы упорного труда. Изучать их начинают в школе и отвечает за это наука химия. В восьмом классе начинается весьма сложная и обширная программа, призванная объяснить школьникам основные понятия всего сущего. Но все-таки больше всего подростков интересуют лабораторные опыты, а не нудные уравнения, в которых необходимо еще и правильно разобраться. Так как малейшая неточность приведет к нарушению структуры какого-либо вещества. Чтобы ребятам было проще адаптироваться и усвоить новые знания, был написан решебник к учебнику «Химия 8 класс Габриелян». Издательский дом «Дрофа», 2013 г.
Что в него включено
Пособие заключает в себе пять глав, что составляет подробнейшие ответы на упражнения по сорока четырем параграфам. ГДЗ предоставляет и доскональный разбор каждого практического задания. На его страницах вы найдете описания и решения следующих типов заданий:
- лабораторные работы;
- практические опыты;
- задачи после каждого параграфа.
Материалы решебника полностью соответствуют действующим федеральным образовательным стандартам и призваны помочь школьникам, независимо от уровня знаний и успеваемости.
Нужен ли решебник
Так как структура решебника полностью повторяет материалы одноименного учебника, учащимся больше не составит труда выполнять практические и домашние задания. Взяв на вооружение данный сборник, восьмиклассники смогут без посторонней помощи педагогов и репетиторов отработать следующие важные навыки:
- Самостоятельный поиск необходимой информации;
- Возможность самопроверки при решении практических заданий;
- Уверенная подготовка к будущим урокам, а также проверочным и контрольным работам.
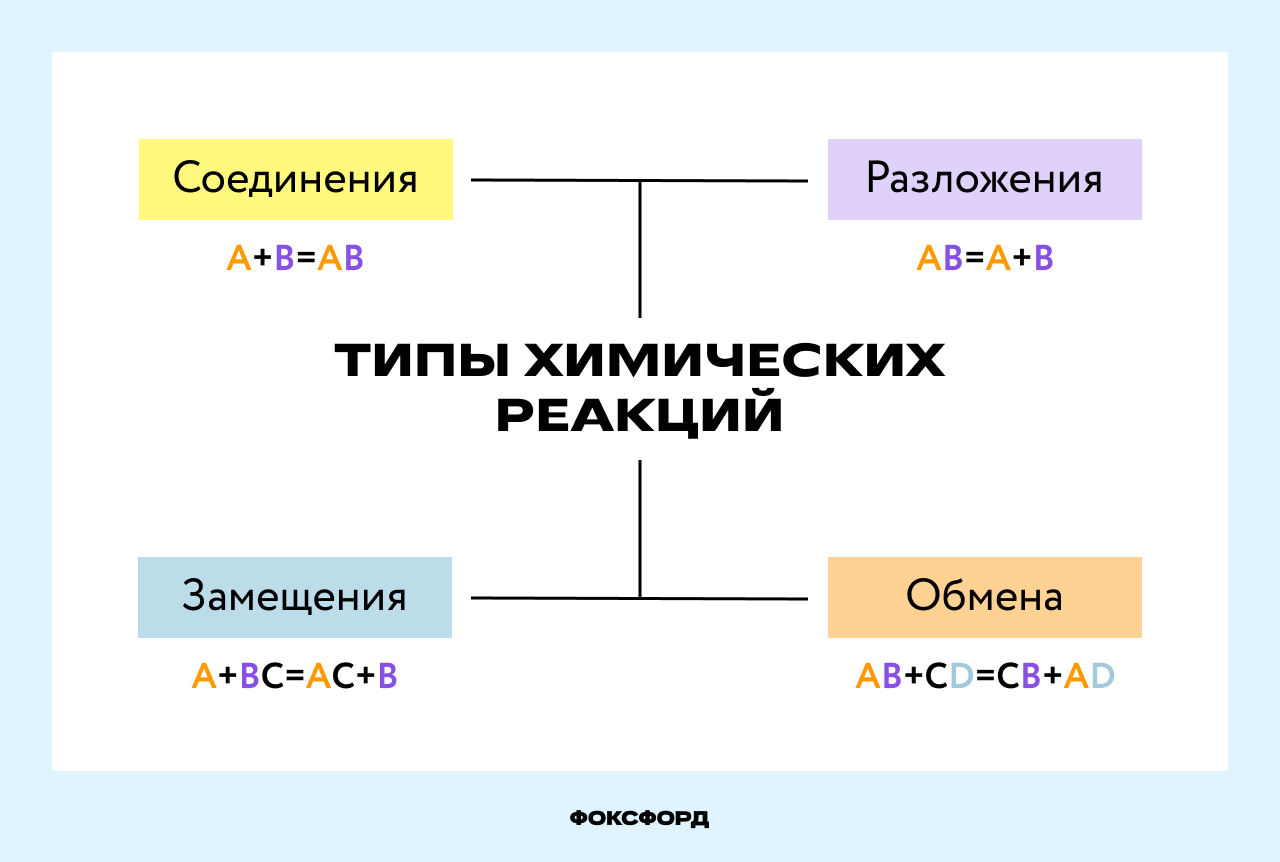
Виды химических реакций
Вещества вступают в реакции по-разному, можно выделить четыре наиболее частых варианта:
Соединение. Два или несколько реагентов образуют один продукт. В реакцию могут вступать как простые вещества, так и сложные. Например, простые вещества водород и кислород взаимодействуют и образуют сложное — воду:
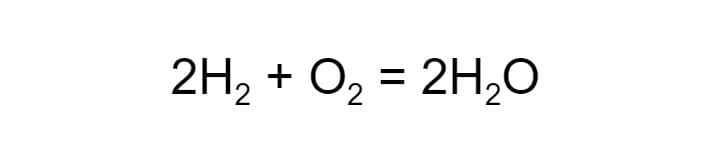
Сложное вещество негашёная известь соединяется с водой, и образуется новое сложное вещество — гашёная известь:
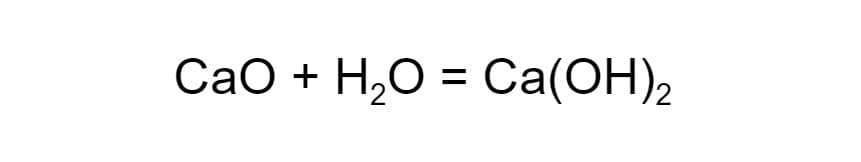
Разложение. Обратный процесс: одно вещество распадается на несколько более простых. Например, если нагреть известняк, получаются негашёная известь и углекислый газ:
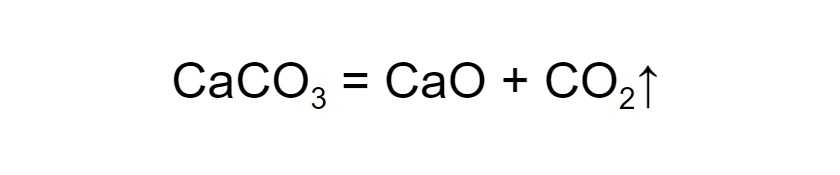
Стрелка вверх означает, что образовался газ. Он улетучивается и больше не участвует в реакции.
Замещение. В реакции участвуют два вещества — простое и сложное. Если атомы химического элемента в простом веществе более активны, они замещают атомы одного из менее активных химических элементов в составе сложного вещества.
В примере атомы цинка замещают атомы водорода в составе хлороводорода, и образуется хлорид цинка:
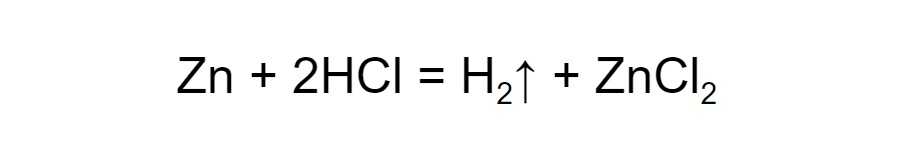
Обмен. Два сложных вещества обмениваются составными частями, в результате получаются два новых сложных вещества. В такой реакции обязательно образуется вода, газ или осадок.
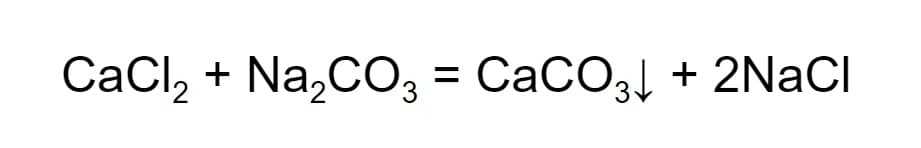
Стрелка вниз означает, что вещество выпало в осадок, поскольку оно нерастворимо.






























